واکنشهای شیمیایی تولید نمک چیست ؟
- طراح سایت
- بدون دیدگاه
واکنشهای شیمیایی گوناگونی وجود دارند که نمک از فراوردههای آن است. برخی از این واکنشها عبارتند از:
- واکنش اسید و باز
- واکنش با اکسیدهای فلزی
- واکنشهای رسوبی
- واکنش با کربنات فلزات
خنثی سازی اسید و باز
نمک بهطور کلی در نتیجه واکنش اسید و باز تشکیل میشود که به واکنشهای «خنثیسازی» (Neutralization) مشهور هستند. در واقع وقتی اسید و باز با هم واکنش میدهند موجب خنثی شدن یکدیگر میشوند. محصول خنثی شدن نیز نمک و آب است.
- محلولهای اسیدی حاوی یونهای هیدروژن (H+)(𝐻+) هستند.
- محلولهای بازی حاوی یونهای هیدروکسید (OH–)(𝑂𝐻–) هستند.
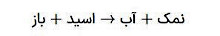
که معادله شیمیایی یونها به صورت زیر رخ میدهد.
H+(aq)+OH–(aq)→H2O(l)𝐻+(𝑎𝑞)+𝑂𝐻–(𝑎𝑞)→𝐻2𝑂(𝑙)
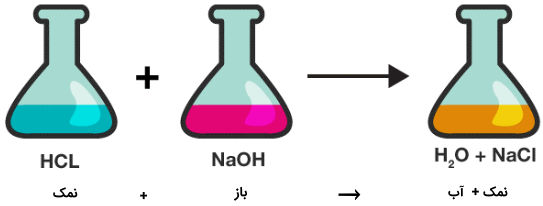
نمکها ترکیبات یونی بوده که از نظر بار الکتریکی بدون بار یا خنثی هستند. باید توجه داشت که نمکهای بدون بار یا خنثی زمانی تشکیل میشوند که واکنش بین اسید و باز قوی یا اسید و باز ضعیف باشد. برای مثال NaCl𝑁𝑎𝐶𝑙 از واکنش اسید قوی HCl𝐻𝐶𝑙 و باز قوی NaOH𝑁𝑎𝑂𝐻 ساخته میشود.
HCl(aq)+NaOH(s)→NaCl(s)+H2O(l)𝐻𝐶𝑙(𝑎𝑞)+𝑁𝑎𝑂𝐻(𝑠)→𝑁𝑎𝐶𝑙(𝑠)+𝐻2𝑂(𝑙)
و واکنش استیک اسید (CH۳COOH)(𝐶𝐻۳𝐶𝑂𝑂𝐻) با آمونیوم هیدروکسید (NH۴OH)(𝑁𝐻۴𝑂𝐻) که اسید و باز ضعیف هستند به صورت زیر انجام میشود و محصول این واکنش، آمونیوم استات (NH۴CH۳CO۲)(𝑁𝐻۴𝐶𝐻۳𝐶𝑂۲) که نمکی بدون بار است.
CH3COOH+NH4OH→CH3COONH4+H2O𝐶𝐻3𝐶𝑂𝑂𝐻+𝑁𝐻4𝑂𝐻→𝐶𝐻3𝐶𝑂𝑂𝑁𝐻4+𝐻2𝑂
یونهای دوقطبی مانند متابولیتها، پپتیدها و پروتئینها در ساختار خود همزمان آنیون و کاتیون دارند ولی در دسته نمکها قرار نمیگیرند. از کاربردهای خنثیسازی اسید و باز را در کارکرد داروهای ضداسید معده میتوان مشاهده کرد. این داروها با اسید اضافی معده واکنش میدهند و آن را خنثی میکنند. نوع نمکی که در طی واکنش خنثیسازی تولید میشود به اسید و باز مورد استفاده بستگی دارد.
- نمکهای کلرید: در نتیجه خنثیسازی هیدروکلریک اسید تولید میشوند.

- نمکهای نیترات: در نتیجه خنثیسازی نیتریک اسیدها تولید میشوند.

- نمکهای سولفات: در نتیجه خنثیسازی سولفوریک اسید تولید میشوند.

- آنچه در این مقاله میخوانیم

- ارسال دیدگاه